Durante décadas, o diagnóstico das demências foi tratado como uma escolha simples: Alzheimer ou Parkinson. Contudo, a neurociência moderna está revelando uma realidade muito mais complexa. A copatologia — presença simultânea de múltiplas doenças neurodegenerativas no mesmo cérebro — está sendo reconhecida como a regra, e não a exceção. Essa descoberta está revolucionando a forma como médicos diagnosticam, tratam e entendem as demências.
Se você já se perguntou por que dois pacientes com o mesmo diagnóstico de Alzheimer apresentam trajetórias tão diferentes, a resposta está justamente na copatologia. Ademais, ela explica por que os tratamentos tradicionais frequentemente não funcionam como o esperado. Entender esse fenômeno é essencial para pacientes, cuidadores e profissionais de saúde.
Neste artigo, são apresentadas as descobertas mais recentes sobre a copatologia nas demências, os pesquisadores que lideram esse campo e o impacto prático no diagnóstico e no tratamento. Ao final, você encontrará um FAQ completo e perguntas para reflexão.
O Que É Copatologia e Por Que Ela Muda Tudo no Diagnóstico das Demências
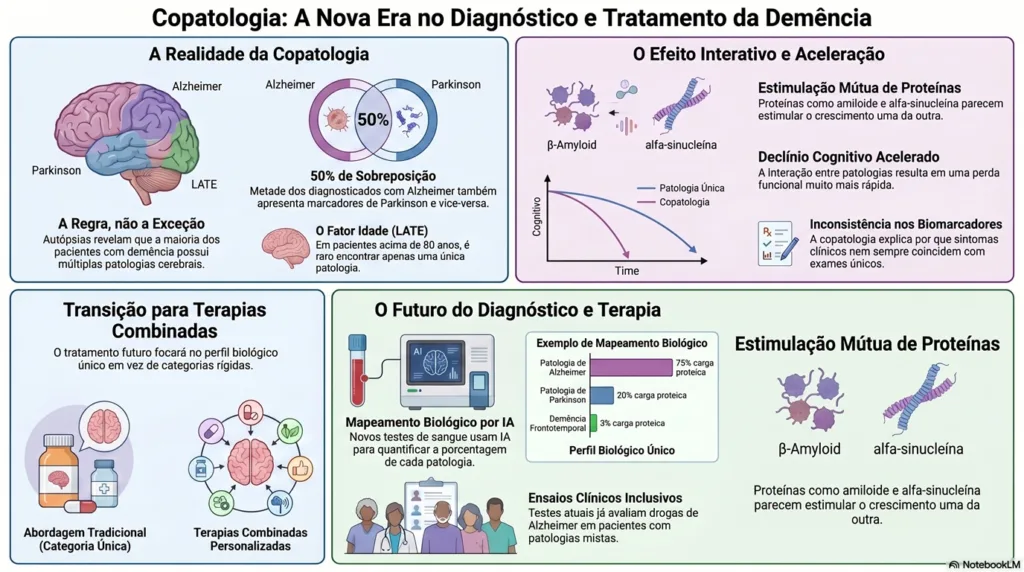
A copatologia é definida como a coexistência de múltiplas patologias neurodegenerativas em um único paciente. Portanto, em vez de apenas uma proteína “vilã”, o cérebro acumula simultaneamente diferentes tipos de proteínas anormais. Isso inclui combinações de beta-amiloide, tau, alfa-sinucleína e TDP-43, cada uma associada a uma doença diferente.
Por muito tempo, o modelo vigente era o de “uma doença, uma proteína”. Segundo esse modelo, o Alzheimer era definido exclusivamente pelas placas de beta-amiloide e pelos emaranhados de tau. Já o Parkinson era identificado pela alfa-sinucleína. Entretanto, esse paradigma está sendo superado de forma definitiva. As evidências de estudos de autópsia demonstraram que a sobreposição é muito mais comum do que se imaginava.
De acordo com a neuropatologista Lea Grinberg, da Mayo Clinic, “a copatologia ajuda a explicar por que os sintomas não batem com os biomarcadores, por que as trajetórias variam tanto e por que os resultados do tratamento não são necessariamente o que esperamos que sejam”. Essa afirmação resume com precisão o impacto clínico desse fenômeno.
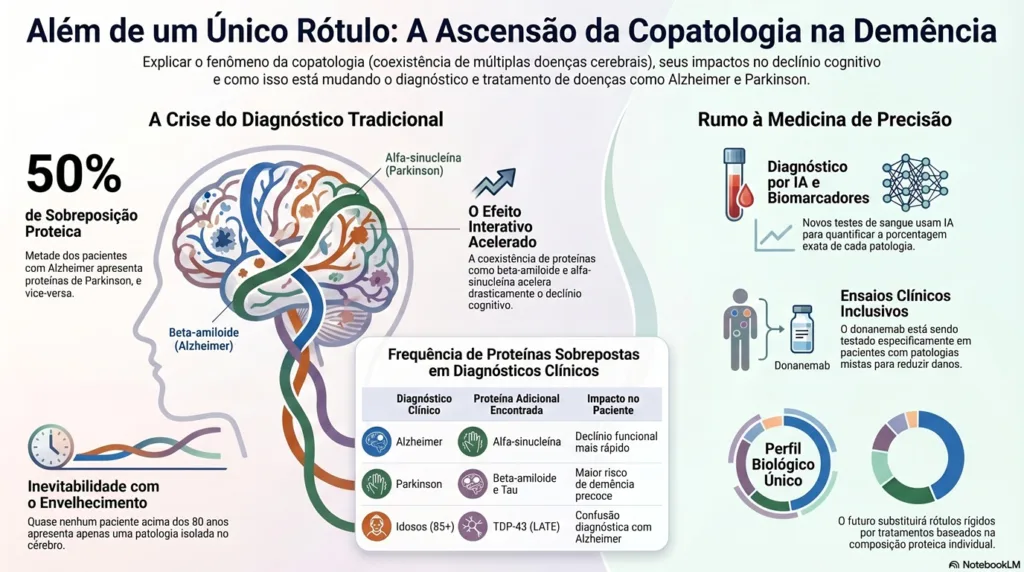
Além disso, as estatísticas são contundentes. Cerca de 50% dos pacientes diagnosticados com Alzheimer também apresentam depósitos de alfa-sinucleína, proteína característica do Parkinson. Da mesma forma, metade dos pacientes com Parkinson que desenvolvem demência exibe níveis elevados de beta-amiloide e tau. Esses dados tornam a copatologia um elemento central na medicina neurológica contemporânea.
A Sobreposição Alzheimer-Parkinson: Dados que Surpreendem os Especialistas
A sobreposição entre as patologias do Alzheimer e do Parkinson é um dos exemplos mais estudados de copatologia. Consequentemente, essa sobreposição tem implicações diretas para o prognóstico dos pacientes. Quanto mais proteínas coexistem, mais complexo e imprevisível tende a ser o quadro clínico.
Estudos realizados com pacientes de Alzheimer familiar — aqueles que desenvolvem a doença precocemente, por volta dos 40 anos — revelaram dados surpreendentes. Metade desses pacientes apresentava Corpos de Lewy (depósitos de alfa-sinucleína) em suas autópsias, mesmo sem diagnóstico prévio de Parkinson. Isso indica que a copatologia não é apenas um fenômeno do envelhecimento avançado.
Por outro lado, pacientes em estágios iniciais do Parkinson também são frequentemente afetados. Nesses casos, níveis elevados do marcador p-tau217 — tipicamente associado ao Alzheimer — foram detectados no sangue. Esse biomarcador se mostrou um poderoso preditor de declínio cognitivo acelerado em pacientes de Parkinson, conforme demonstrou o neurologista Tom Tropea.
Esse conjunto de evidências sugere que as fronteiras entre as doenças neurodegenerativas são muito mais porosas do que se acreditava. Portanto, o diagnóstico preciso exige uma abordagem biológica abrangente, e não apenas a identificação de uma proteína isolada.
Veja abaixo uma comparação entre o modelo tradicional e o novo paradigma da copatologia:
- Foco molecular: De uma única proteína “de assinatura” para um perfil biológico múltiplo e combinado.
- Categorização: De diagnósticos rígidos (ex: “É Alzheimer”) para descrições baseadas em carga patológica percentual.
- Etiologia do declínio: De uma patologia isolada para a interação e sinergia proteica.
- Abordagem terapêutica: De droga única para um alvo específico para terapias combinadas e personalizadas.
O Efeito Interativo: Quando a Copatologia Acelera o Declínio Cerebral
A presença simultânea de múltiplas proteínas não é uma mera coincidência estatística. Na verdade, essas proteínas parecem estimular ativamente umas às outras, criando um ciclo vicioso de destruição neuronal. Esse fenômeno foi denominado “efeito interativo” pela neurologista Sharon Sha, da Universidade de Stanford.
O mecanismo funciona da seguinte forma. Primeiro, a proteína beta-amiloide começa a se acumular no tecido cerebral. Em seguida, ela age como um “molde” ou gatilho, estimulando o dobramento incorreto da alfa-sinucleína. A interação entre essas duas proteínas intensifica a toxicidade celular. Por fim, os neurônios são destruídos em um ritmo muito superior ao de qualquer patologia isolada.
Assim, o resultado clínico é devastador: um declínio funcional e cognitivo acelerado, que encurta significativamente o período de independência do paciente. Isso explica por que alguns pacientes declinam muito mais rapidamente do que outros com o mesmo diagnóstico inicial.
Os pesquisadores estão atualmente em busca do que chamam de “Hipótese da Via Comum”. A ideia central é que existe uma origem ou via metabólica ainda desconhecida nos neurônios, responsável por impulsionar essa cascata de múltiplas patologias. Encontrar essa via poderia representar um salto revolucionário no tratamento das demências. Uma única terapia poderia, assim, interromper vários processos degenerativos de uma só vez.
LATE: A Doença Invisível nos Cérebros Mais Idosos
Para pessoas acima de 85 anos, a complexidade da copatologia aumenta consideravelmente com a presença de uma condição pouco conhecida: a LATE. A sigla refere-se à Encefalopatia TDP-43 Relacionada à Idade com Predominância Límbica. Ela é caracterizada pelo acúmulo da proteína TDP-43, também observada em certas formas de demência frontotemporal.
A LATE é considerada quase onipresente em cérebros muito idosos. Especialistas são categóricos ao afirmar que é extremamente raro encontrar apenas uma patologia em indivíduos com mais de 80 anos. Consequentemente, a LATE quase sempre coexiste com outras doenças, especialmente o Alzheimer.
O grande desafio clínico é que a LATE mimetiza os sintomas do Alzheimer, tornando o diagnóstico diferencial muito difícil sem exames específicos. Além disso, o tratamento direcionado à proteína amiloide — principal alvo das novas terapias para Alzheimer — não tem qualquer efeito sobre a TDP-43. Portanto, um paciente pode estar sendo tratado apenas para uma fração do problema real.
Abaixo, confira o perfil das principais proteínas envolvidas na copatologia:
- Beta-amiloide e Tau: Marcadores centrais do Alzheimer. Frequentemente coexistem com patologias de Parkinson e LATE.
- Alfa-sinucleína: Proteína característica do Parkinson e da Demência com Corpos de Lewy. Presente em metade dos casos de Alzheimer; acelera o declínio motor e cognitivo.
- TDP-43: Proteína da LATE e da Demência Frontotemporal. Mimetiza o Alzheimer em pacientes muito idosos (acima de 85 anos).
- p-tau217: Marcador crítico de declínio funcional. Prediz trajetória acelerada em pacientes de Parkinson, conforme demonstrado pelo neurologista Tom Tropea.
Diagnóstico Vivo da Copatologia: Da Autópsia ao Exame de Sangue
Historicamente, a copatologia só era confirmada após a morte, por meio de autópsias. Hoje, pesquisadores estão desenvolvendo tecnologias inovadoras que prometem identificar essas sobreposições em pacientes vivos. É importante ressaltar, entretanto, que essas tecnologias são ainda experimentais e precisam de validação clínica em larga escala antes de estarem disponíveis ao público em geral.
O neurologista Richard Mayeux, da Universidade de Columbia, utiliza vesículas extracelulares — partículas ricas em proteínas liberadas pelos neurônios no sangue. Por meio dessa análise, é possível detectar biomarcadores de Alzheimer, Parkinson, LATE e doenças vasculares cerebrais simultaneamente. Trata-se de uma espécie de “biópsia líquida” do cérebro, minimamente invasiva.
Já o pesquisador Carlos Cruchaga, da Universidade Washington, desenvolveu um painel experimental com 15 marcadores proteicos, analisados por inteligência artificial. O teste é capaz de quantificar a composição da doença em termos percentuais. Por exemplo: 75% de patologia de Alzheimer, 20% de Parkinson e 5% de demência frontotemporal. Esse tipo de mapeamento seria impensável há apenas uma década.
Além disso, o marcador sanguíneo p-tau217 está sendo estudado como um “oráculo prognóstico”. Níveis elevados dessa proteína em pacientes com Parkinson predizem um declínio cognitivo e funcional muito mais rápido. Curiosamente, esse sinal aparece antes mesmo dos sintomas clínicos, abrindo uma janela de oportunidade para intervenções precoces.
Os benefícios práticos desse avanço diagnóstico são significativos:
- Fim da incerteza: Alinhamento entre os sintomas observados e os resultados dos exames.
- Prognóstico personalizado: Capacidade de prever a agressividade da doença com base no perfil proteico.
- Seleção terapêutica precisa: Escolha de tratamentos que correspondam à biologia individual do paciente.
- Intervenção precoce: Identificação de risco antes do surgimento dos sintomas clínicos.
Tratamento Personalizado: O Futuro É um Perfil Biológico, Não um Rótulo
O reconhecimento da copatologia traz um dilema ético e clínico importante. Vale a pena remover a proteína amiloide se a alfa-sinucleína ou a TDP-43 continuarem presentes? A resposta da medicina atual é pragmática: é melhor remover o que é tratável do que não remover nada. Essa lógica é chamada de “Teoria de Redução de Carga”.
Um marco nessa direção é o ensaio clínico com o medicamento donanemab, liderado pela neurologista Sharon Sha, da Universidade de Stanford. Este é o primeiro grande estudo a incluir intencionalmente pacientes com patologias mistas — especificamente Alzheimer e Corpos de Lewy. O objetivo é verificar se a remoção da carga amiloide pode interromper o “efeito interativo” e amenizar os sintomas de forma global.
A lógica clínica por trás dessa abordagem é de empatia pragmática. Mesmo que não seja possível tratar todas as frentes simultaneamente, reduzir a carga proteica total pode dar ao cérebro o “fôlego” necessário para funcionar melhor por mais tempo. Isso representa uma mudança fundamental na filosofia do tratamento das demências.
O neuropatologista Johannes Attems projeta o futuro da seguinte forma: no futuro, não falaremos apenas em “Doença de Alzheimer”. O diagnóstico será um perfil detalhado: “você tem 60% de amiloide, 20% de tau, 15% de TDP-43 e 5% de dano vascular — e aqui está o coquetel para o seu perfil específico”. Essa visão representa a medicina de precisão neurodegenerativa em sua forma mais avançada.
Estratégias
As estratégias terapêuticas que estão sendo desenvolvidas incluem:
- Terapias combinadas: Uso simultâneo de drogas para Alzheimer, Parkinson e proteção vascular, conforme o perfil proteico do paciente.
- Alvos em vias comuns: Medicamentos que tratem a origem celular do estresse proteico, em vez de proteínas isoladas.
- Polifarmácia de precisão: Combinação de fármacos ajustada à porcentagem de cada patologia identificada nos exames.
- Intervenção precoce: Tratamento iniciado antes dos sintomas clínicos, com base nos biomarcadores sanguíneos.
Impacto na Prática Clínica: O Que Muda para Pacientes e Cuidadores
Para pacientes e familiares, entender a copatologia muda a forma de interpretar o diagnóstico e as expectativas de tratamento. Em primeiro lugar, é fundamental compreender que um diagnóstico de Alzheimer não exclui outras patologias coexistentes. Da mesma forma, sintomas atípicos ou progressão mais rápida do que o esperado podem indicar uma sobreposição de doenças.
Além disso, a variabilidade nas trajetórias de declínio — muitas vezes fonte de angústia para as famílias — tem uma explicação biológica concreta. O perfil de copatologia de cada paciente é único. Portanto, comparações com outros pacientes com o mesmo diagnóstico podem ser enganosas e até prejudiciais ao bem-estar emocional dos cuidadores.
Do ponto de vista prático, é recomendável que pacientes e familiares discutam com seus médicos a possibilidade de exames mais abrangentes. A inclusão de biomarcadores como o p-tau217 pode fornecer informações valiosas sobre o prognóstico. Ademais, à medida que os ensaios clínicos como o do donanemab avançam, novas opções terapêuticas podem se tornar acessíveis.
Outro aspecto importante é a escolha de centros especializados. Instituições como a Mayo Clinic, a Universidade de Stanford, a Universidade de Columbia e a Universidade Washington estão na vanguarda da pesquisa em copatologia. Pacientes com casos complexos podem se beneficiar da avaliação por equipes multidisciplinares nessas instituições ou em centros de referência com acesso a protocolos atualizados.
A Ciência que Vem por Aí: Perspectivas para os Próximos Anos
O campo da copatologia está avançando rapidamente. Nos próximos anos, espera-se que diversas tecnologias passem da fase experimental para a prática clínica. O painel de 15 marcadores com inteligência artificial, desenvolvido por Carlos Cruchaga, é um dos mais promissores. Contudo, sua validação em larga escala ainda está em curso.
Da mesma forma, as vesículas extracelulares estudadas por Richard Mayeux representam uma fronteira importante na biópsia líquida cerebral. Essa tecnologia pode transformar o diagnóstico de copatologia em um exame de rotina, acessível e minimamente invasivo. Por enquanto, entretanto, seu uso permanece restrito a centros de pesquisa.
Paralelamente, a busca pela “via comum” nos neurônios está ganhando força. Se essa via for identificada, um único medicamento poderia interromper a cascata de múltiplas proteínas anormais. Isso tornaria obsoletas as categorias diagnósticas atuais. Consequentemente, toda a estrutura dos ensaios clínicos precisaria ser redesenhada.
Finalmente, é importante destacar que os avanços nessa área têm impacto direto na qualidade de vida das populações mais idosas. Com o envelhecimento global acelerado, o número de pessoas afetadas por demências com copatologia tende a crescer significativamente. Portanto, investir em diagnóstico preciso e tratamento personalizado é também uma questão de saúde pública.
Perguntas para Reflexão e Interação dos Leitores
A copatologia levanta questões importantes que ainda estão sendo debatidas na comunidade científica e entre pacientes. Você já conversou com um médico sobre a possibilidade de copatologia no caso de um familiar com diagnóstico de demência? Você acredita que o sistema de saúde do seu país está preparado para adotar uma medicina de precisão neurodegenerativa? Como a perspectiva de um diagnóstico por “perfil biológico” muda sua forma de encarar a demência?
Deixe sua opinião e suas dúvidas nos comentários abaixo. Sua experiência pode ajudar outras famílias que enfrentam desafios semelhantes.
FAQ: Perguntas Frequentes sobre Copatologia nas Demências
É a presença simultânea de múltiplas doenças neurodegenerativas no mesmo paciente. Por exemplo, um paciente pode ter Alzheimer e Parkinson ao mesmo tempo, com proteínas de ambas as doenças coexistindo no cérebro.
Sim. Estudos de autópsia mostram que até 50% dos pacientes com Alzheimer também têm alfa-sinucleína, proteína do Parkinson. Em pessoas acima de 80 anos, é raro encontrar apenas uma patologia cerebral.
É o fenômeno pelo qual diferentes proteínas patológicas se estimulam mutuamente, acelerando a destruição neuronal. A beta-amiloide, por exemplo, estimula o acúmulo de alfa-sinucleína, tornando o declínio cognitivo mais rápido e agressivo.
LATE é a Encefalopatia TDP-43 Relacionada à Idade com Predominância Límbica. É caracterizada pelo acúmulo da proteína TDP-43 e é muito comum em pessoas acima de 85 anos. Frequentemente mimetiza o Alzheimer, dificultando o diagnóstico diferencial.
Existem biomarcadores como o p-tau217 e tecnologias em desenvolvimento, como vesículas extracelulares e painéis com inteligência artificial. Contudo, essas tecnologias ainda são experimentais e precisam de validação clínica para uso em larga escala.
Donanemab é um anticorpo monoclonal que age removendo a proteína beta-amiloide do cérebro. Um ensaio clínico liderado por Sharon Sha, de Stanford, está testando o donanemab especificamente em pacientes com copatologia (Alzheimer + Corpos de Lewy), para verificar se a redução da carga amiloide melhora os sintomas globais.
Não necessariamente. A lógica atual é que remover o que é tratável — como a amiloide — é melhor do que não fazer nada. Contudo, o campo avança para terapias combinadas que abordem múltiplas proteínas simultaneamente.
O pesquisador Carlos Cruchaga, da Universidade Washington, desenvolveu um painel experimental que usa IA para analisar 15 marcadores proteicos no sangue. O sistema quantifica percentualmente a presença de cada patologia, como 75% Alzheimer e 20% Parkinson.
Não. Estudos com pacientes de Alzheimer familiar — que desenvolvem a doença aos 40 anos — mostram que metade apresenta Corpos de Lewy. Portanto, a copatologia pode ocorrer em adultos mais jovens com formas genéticas de demência
É a teoria de que existe uma origem ou via metabólica ainda desconhecida nos neurônios que impulsiona o acúmulo de múltiplas proteínas patológicas ao mesmo tempo. Identificar essa via poderia levar ao desenvolvimento de uma terapia capaz de tratar várias doenças neurodegenerativas simultaneamente.
#Copatologia #Alzheimer #Parkinson #Demência #MedicinaDePrec isão #Neurologia #SaúdeCerebral #TDP43 #LATE #Donanemab #BiomarkersDemência #EfeitoInterativo #NeurociênciaModerna #EnvelhecimentoCerebral #DemênciaFrontotemporal #CorposDeLewy #ptau217 #AlfaSinucleína #SharonSha #LeaGrinberg


Comentários recente